| 訊息: |
|
|
|
|
可泰利Cotellic/cobimetinib
大腸直腸癌即時照護網 present in 2017/01/04
仿單連結:可泰利(黑色素瘤)
編修自仿單及文獻
可泰利 Cotellic/cobimetinib (1顆 20 毫克)
是高度選擇的MEK1 及MEK2 酪胺酸-蘇胺酸激酶之標靶抑制劑。
#### 2017/01/05 台灣的適應症 ####
Cotellic 與Zelboraf 併用於治療BRAF V600 突變陽性且無法以手術切除或轉移性的黑色素瘤患者。
==標準劑量
Cotellic 建議劑量為60 毫克 (三顆),一天1 次。Cotellic治療以28 天為一週期。每一治療週期包括連續服用21 天(治療期:第1 天至第21天),一天1 次,每次三顆20 毫克錠劑(60 毫克);之後停止服用Cotellic 7 天(治療休息期:第22 至第28 天)。每次服用三顆20 毫克錠劑(60 毫克)可與食物併服或空腹服用。Cotellic 錠劑應搭配開水整顆吞服。如果出現Cotellic 所導致的心臟症狀且Cotellic 暫時停藥後仍未改善,應考慮停止Cotellic 的治療。(臨床使用常需調整劑量)
==不良反應
左心室功能受損(心臟射出分率降低),斑丘疹,痤瘡狀,皮膚炎,腹瀉,噁心,嘔吐,貧血,脈絡膜視網膜病變(漿液性視網膜病變(Serous retinopathy)),視力模糊,視網膜剝離,發燒,發抖,脫水,低血鈉症,基底細胞癌,光敏感,血管異常,高血壓, 高血糖症,低血磷, 肺炎, 出血, 肝功能異常,血膽紅素升高, CPK 升高....等。
==代謝/排除
經由CYP3A 進行氧化和經由UGT2B7 進行葡萄糖醛酸化似乎是cobimetinib 代謝的主要途徑。Cobimetinib 大量地被代謝並經由糞便排除。口服cobimetinib 後的平均排除半衰期為43.6 小時(範圍23.1 至69.6 小時)。
####在大腸直腸癌的臨床試驗:參考用,因為經驗有限####
針對治療微衛星穩定性的大腸直腸癌: Atezolizumab (抑制 PD-L1的抗體)。 Phase Ib 的臨床試驗,使用了 cobimetinib 加上atezolizumab 雙重療法測試於有晚期大腸直腸癌的療效.
試驗方式:
cobimetinib 的劑量由 20mg/day 逐步上升測試到 60 mg/day (21天療程/7天休息),搭配每兩個星期使用靜脈注射給藥 800 mg 的 Atezolizumab 合併使用.
試驗結果:
截至 2015 年 10 月 12 號為止,有 23 位大腸直腸癌病患 (22 位 KRAS 基因突變,一位KRAS基因沒有突變)最常見的與治療相關的副作用反應為腹瀉(69.6%), 疲憊(52.2%),痤瘡性皮炎(43.5%), 皮膚紅疹(34.8%),斑性丘狀發疹(26.1%),瘙癢(26.1%) 與噁心(26.1%).因治療引起的Grade 3-4 副作用的比例大約為34.8%.在這些因治療引起的 Grade 3-4 副作用中,有發生於兩個人以上的是腹瀉(8.7%).沒有發Grade 5 的副作用(治療導致死亡).整體腫瘤反應率(overall response rate)為17% (4位部分有效) ,整體腫瘤穩定率(stable disease rate)為22 % (5 位疾病穩定).
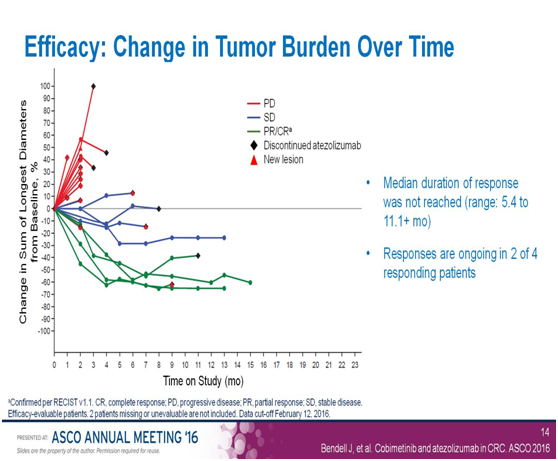
HWT@2018/7/9
但是隨後正式臨床試驗:IMblaze370的結果是 研究失敗)
研究將363例患者轉移性大腸直腸癌以2:1:1的比例隨機分配至atezolizumab加cobimetinib(n = 183),atezolizumab單獨(n = 90)或單藥regorafenib(n = 90)。 大多數患者的微衛星穩定(MSS; 89%至93%)。 在IMblaze370 III期研究中,PD-L1抑製劑atezolizumab與MEK抑製劑cobimetinib聯合應用的中位OS為8.9個月(95%CI,7.00-10.61),而多激酶抑製劑regorafenib為8.5個月(HR,1.00; 95%CI,0.73-1.38; P = .9871)。 對於atezolizumab單藥治療,中位OS為7.1個月(95%CI,6.05-10.05),與regorafenib相比風險比為1.19(95%CI,0.83-1.71; P = .3360)。
HWT@20180904
新的用法
FDA已批准BRAF抑製劑 encorafenib(Braftovi),MEK抑製劑 binimetinib(Mektovi)和 EGFR抑製劑 西妥昔單抗(爾必得舒)(Erbitux)聯合用於治療 BRAF V600E突變型 轉移性結直腸癌患者在轉移性處方中對1或2個先前治療失敗之後。
FDA根據正在進行的隨機3期 BEACON CRC試驗的數據:
30例轉移性結直腸癌患者接受了encorafenib加binimetinib和西妥昔單抗。 29名患者患有BRAF V600E突變腫瘤。結果顯示完全成熟的整體存活 (Overall Survival) 數據為12.6個月。在分析時尚未達到中位整體存活。 中位無惡化存活期 Progression Free Survival PFS 為8個月(95%CI,5.6-9.3)。研究人員觀察到總體反應率為 overall response rate 48%(n = 17),1年存活率 62%。 三聯體組合似乎副作用耐受良好。最常見的3級或4級不良事件包括疲勞(13%),貧血(10%),血肌酸激酶增加(10%)和天冬氨酸氨基轉移酶增加 (肝功能)(10%)。